经过这么多年对化学的学习,要是你至今仍然依靠背诵口诀去判别反应类型,那么在高考当中就有可能会遭遇不利的情况了。对于氧化还原反应而言,不能够仅仅依据是否有单质参与来判断,唯独可以依据化合价是否发生变化来做出判断;溴水出现褪色的现象,其原因并不一定就是存在双键或者三键,醛类以及酚类物质在这个方面同样能够达成使溴水褪色的效果。要是这些细节无法清晰地弄明白,那么在选择题当中一旦出现错误,每次失分就是3分。
氧化还原反应判定的唯一标准
其本质为氧化还原反涉及元素化合价出现变化,与是否存在单质参与毫无关联,众多同学被初中老师所教授的“有单质参加便属于氧化还原”这一内容严重误导了。
处于同素异形体状态的物质之间所发生的转化情况,举例来说就如同氧气转变为臭氧、白磷转变为红磷此类情况,这些反应过程当中均有单质参与其中,然而化合价从始至终都未曾发生改变,所以该类反应并非属于氧化还原反应范畴。与之相反的情况,就像二氧化氮溶解于水从而生成硝酸以及一氧化氮这种情况,此反应过程中并没有单质参与进来,但是氮元素的化合价却发生了变化,这种情况反而属于典型的会发生氧化还原的反应。
溴水褪色的多种可能性
在有机化学范畴之中,溴水出现褪色这种情况乃是一个高频考点,然而千万不要错误地认为,仅仅只有碳碳双键或者碳碳叁键才能够致使它出现褪色现象。醛类物质举例来说像乙醛,是能够与溴水发生氧化反应的这种状况,进而使得溴水出现褪色的这种结果。
苯环上带有酚轻基的酚类化合物更具典型性,苯酚与溴水发生反应后会生成三溴苯酚这种白色沉淀,与此同时溴水颜色逐渐褪去。该反应属于取代反应,跟分子结构中不饱和键并无关系。所以一旦看到溴水褪色就匆忙去写双键相关内容,在2024年高考中肯定是要丢分的。
基本反应类型的模糊地带
四种基本反应类型,也就是化合、分解、置换以及复分解,并不能够将所有的化学反应都包括进去。浓硫酸跟硫化氢发生反应,从而生成硫单质,这既不属于置换反应,也不属于复分解反应。二氧化氮与氢氧化钠溶液发生反应,进而生成硝酸钠跟亚硝酸钠,同样是不属于基本反应类型的。
碳单质参与和浓硫酸、浓硝酸的反应,会生成多种产物,这些反应在教材当中被归类为氧化还原反应,然而要是硬套基本反应类型就会出现问题,在做题的时候碰到这种情况,要果断跳出初中思维。
化学平衡移动的多因素分析
剖析化学平衡问题之际,温度、浓度、压强予以同时发生变化的状况可是最令人头疼不已的。举例来说,于硫化氢水溶液当中添加硫酸铜,进而生成硫化铜沉淀,如此一来这会致使H2S电离平衡朝着右边进行移动,其后果便是H+浓度反倒增大,并非是所有离子浓度均减小。
运用假设之法可使思路得以厘清:首先假定其他条件维持不变,对第一个因素的影响展开剖析,接着再考量第二个因素。当对硫化氢溶液实施稀释操作时,先是假设平衡并不发生移动,浓度变为原来的一半,随后再思考平衡朝着右方移动,最终得出 S2-浓度相较于稀释之前还要大,此结论众多人难以想到。
水电离的H+和OH-恒等关系
在电解质溶液里,水电离出的H⁺与OH⁻ 的浓度始终相等,这可是解题的窍门所在。于硫化钠溶液当中,当pH等于10时, 此时c(H⁺) 为10的负10次方mol/L , 然而这是溶液里H⁺ 的浓度,并非由水电离产生的。水电离出的H⁺ 一部分被S²⁻ 结合进而生成了HS⁻。
其实际水电离出来的OH-浓度为10^-4 mol/L所示,故而水电离的H+同样是10^-4 mol/L。酸溶液里面OH-均源自水,能够发生水解的盐溶液之中H+以及OH-皆来自水,紧紧把握住这个来源去辨析,2023年江苏卷的那道离子浓度题目便能够顺利解决。
有机物结构与性质的关联
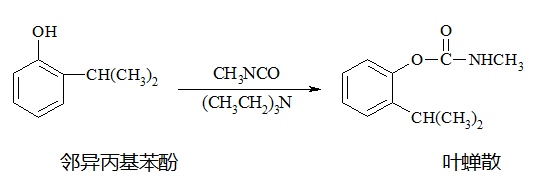
官能团对有机物性质起决定作用,但碳链以及官能团位置所产生的影响也需予以关注。叶蝉散这类农药 ,苯环在催化剂存在的情况下能够与氢气发生加成反应 ,然而酯基和肽键却不具备这样的性质。于是 ,当邻异丙基苯酚与叶蝉散以等物质的量与氢气进行反应时 ,二者的消耗量存在差异 ,前者是苯环进行加氢反应 ,后者除了苯环加氢之外还有羰基的相关反应。
查验叶蝉散里头有无邻异丙基苯酚,借助氯化铁溶液瞧瞧是否呈现紫色挺可靠,然而采用酸性高锰酸钾却不行,缘由在于叶蝉散自身或许含有不饱和键,这会致使高锰酸钾褪掉颜色。酚类物质的邻对位取代准则,于推断同分异构体之际格外关键,像苯酚和溴起反应,仅考量邻对位,可是书写同分异构体务必将间位也纳入考量范围。
在你做题期间,碰到过最为坑人的化学判断题是哪一个,于评论区域分享出来,从而让大伙一块儿避开雷区,要是觉着有用的话,记住顺手点赞做好收藏,及至下次参加考试之前,把它翻找出来瞧瞧。